视网膜病变(专业版)
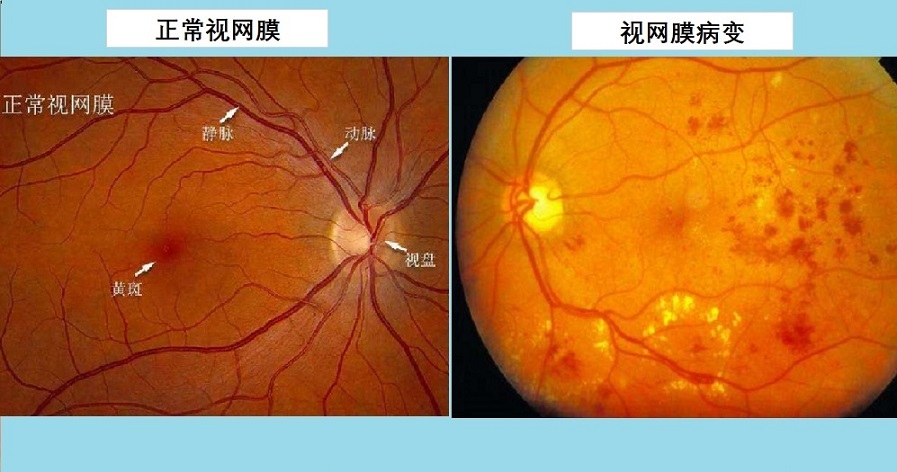
视网膜病变即视网膜损伤,如不治疗和控制可严重和永久性损害视力,甚至导致失明。
其他名称:视网膜受损;视网膜病
英文名称:Retinopathy,Retinal damage,Retinal Disease
然而,许多糖尿病视网膜病变的早期迹象,可由医生检查出来。
当出现症状时,可能会出现宽谱视力问题,从轻度模糊到突然剧烈的视力损失,特别是在视网膜脱离或出血的情况下。
综合疗法可包括如下:
调整饮食与生活方式
营养与草本综合干预
以下是基于循证医学和循证营养学有关文献综合的结果。
有助于防控视网膜病变营养和草本补充剂,主要包括如下:
1.苯磷硫胺:
苯磷硫胺是硫胺素(维生素B1)的衍生物。它已被证明可以减少AGEs(糖基化终产物)引发的视网膜和全身损伤1。
在糖尿病的动物模型中,苯磷硫胺给药通过改善炎症和减轻因高血糖导致的组织损伤的各种途径来预防糖尿病视网膜病变2。在另一种糖尿病动物模型中,苯磷硫胺和硫胺素能够减少视网膜和其他组织中AGEs的积聚3。在1型糖尿病患者中,每天二次补充300mg苯磷硫胺和600mg α-硫辛酸,持续28天,也被证明可以减少的AGEs积累4。
2.欧米伽-3脂肪酸:
包括欧米伽-3脂肪酸在内的多不饱和脂肪酸在身体中发挥着许多作用。有一些证据表明,ω-3脂肪酸可能在维持视网膜健康方面发挥关键作用5。DHA(一种主要的ω-3脂肪酸)在视网膜中含量很高,视网膜中DHA水平的降低与视网膜功能的改变有关。即使在DHA摄入量较低的时期,视网膜中的DHA水平也会保持不变,这进一步强调了其在视网膜组织中的重要性6。
DHA具有抗炎特性,可能能够抵消糖尿病视网膜病变中出现的一些炎症变化7,8。此外,DHA是一种名为神经保护素D1的化合物的前体,该化合物保护眼睛免受炎症损伤,并促进视网膜内细胞的存活9,10。神经保护素D1还抑制新血管的生长7。DHA本身也可以对抗视网膜中异常血管的生长11。在糖尿病动物模型中,补充ω-3有助于预防糖尿病视网膜病变12,13。
ω-3脂肪酸也可能在早产儿视网膜病变中发挥作用。在妊娠晚期,大量长链多不饱和脂肪酸通过胎盘转移到胎儿体内。早产时,婴儿的储备可能不足,这可能会影响视网膜发育14。在早产儿视网膜病变的动物模型中,在饮食中补充ω-3脂肪酸可以防止异常血管发育和视网膜病变5,14-16。一项临床试验发现,接受静脉注射富含ω-3脂肪酸的鱼油的早产儿需要视网膜病变的激光手术较少17。
3.类胡萝卜素和维生素A:
维生素A和类胡萝卜素的相关化合物对眼睛健康和功能至关重要。维生素A及其前体β-胡萝卜素是眼睛细胞吸收光线所必需的。其他类胡萝卜素,包括叶黄素、玉米黄质和番茄红素,也存在于眼睛中,对正常视力和保护眼睛免受潜在的破坏性光线和氧化应激至关重要18,19。多项研究发现,与没有视网膜病变的糖尿病患者相比,糖尿病视网膜病变患者的番茄红素、叶黄素和其他类胡萝卜素水平较低18-20。
研究已经调查了维生素A和其他类胡萝卜素作为潜在的视网膜病变治疗方法。一项临床试验发现,患有非增殖性视网膜病变的糖尿病患者在连续三个月每天补充6mg叶黄素和0.5mg玉米黄质后,视力有所改善19。一项临床试验发现,至少两周内肌肉注射10,000IU维生素A有助于改善早产儿的视网膜敏感性,进一步支持维生素A对视网膜损伤的潜在保护作用21。
4.锌:
锌在眼部含量浓度较高,可以帮助减少眼睛的氧化损伤22。糖尿病视网膜病变患者的锌水平通常低于健康人23,24。补充锌可能有助于预防糖尿病视网膜病变并延缓其进展。锌还有助于改善血糖控制,抑制异常视网膜血管的生长,防止血管受损和渗漏24。在糖尿病大鼠模型中,补锌抑制了VEGF的水平,VEGF是一种参与新生血管形成的化学物质24。
5.硫辛酸:
硫辛酸是一种“万能”的抗氧化剂,已知可提高2型糖尿病患者的胰岛素敏感性,并能预防糖尿病视网膜病变25。它可以帮助恢复视网膜细胞内的抗氧化防御26。对糖尿病动物模型的研究发现,给予α-硫辛酸可以减少被自由基损伤的分子的积累,并有助于保护视网膜中的血管27,28。硫辛酸似乎还能抑制参与新血管形成的生长因子的产生,这是糖尿病视网膜病变进展的主要特征25。
6.肌肽:
肌肽是一种主要由骨骼肌产生的化合物,由两种氨基酸(丙氨酸和组氨酸)组成。它能够阻断AGEs的产生,减轻氧化应激和糖尿病的其他并发症29。
在糖尿病视网膜病变的动物模型中,肌肽补充剂除了抑制AGEs外,还通过其他机制延缓白内障的形成,保护视网膜毛细血管免受高血糖损伤。例如,研究人员发现肌肽的保护作用与预防高血糖诱导的一种名为Ang-2的生长因子增加有关(Ang-2与VEGF结合会导致血管损伤和新生血管形成)30,31。在另一种糖尿病视网膜病变模型中,肌肽与白柳树皮提取物、α-硫辛酸和银杏叶联合保护视网膜细胞免受损伤32。
7.维生素B族:
维生素B12可能通过帮助保持低同型半胱氨酸水平来预防视网膜病变。同型半胱氨酸是一种会损伤血管的氨基酸。糖尿病患者对高同型半胱氨酸水平(高血同)引起的血管损伤特别敏感,因为糖尿病会导致同型半胱氨酸的化学变化,使该分子毒性更强33。中和同型半胱氨酸的酶需要维生素B12才能发挥作用;因此,维生素B12缺乏会导致同型半胱氨酸水平升高,并导致糖尿病视网膜病变34。
患有糖尿病视网膜病变的人通常具有较高的同型半胱氨酸水平和较低的维生素B12水平,这表明维生素B12缺乏与糖尿病视网膜病变之间存在联系33,34。一项研究发现,增殖性糖尿病神经病变患者的同型半胱氨酸水平估计比对照组高出约30%35。在对300名2型糖尿病受试者进行的一项类似研究中,维生素B12和叶酸水平较低与同型半胱氨酸水平升高有关,而在患有糖尿病视网膜病变的研究人群中,同型半胱氨酸的水平尤其高34。另一项研究发现,614名患有视网膜血管疾病的受试者的血浆总同型半胱氨酸水平高于762名对照受试者36。
重要的是,一些糖尿病治疗药物,如二甲双胍可能引起维生素B12下降,增加同型半胱氨酸水平。这种与治疗相关的维生素B12缺乏可能会增加糖尿病视网膜病变的风险,这突出了糖尿病患者补充维生素B12的重要性37。其他B族维生素也可能在预防糖尿病视网膜病变方面发挥协同作用。一项研究发现,维生素B12、叶酸和5’-磷酸吡哆醛(活性维生素B6)的组合在减少非增殖性糖尿病视网膜病变患者的视网膜水肿和提高光敏感性方面具有有益效果38。
8.碧萝芷:
碧萝芷是从法国海松树皮中分离的提取物,已被研究用于治疗糖尿病视网膜病变39。碧萝芷的一个好处是它可以帮助降低血糖水平。此外,碧萝芷可以保护视网膜中的毛细血管免受损伤。
一项研究77名2型糖尿病患者的临床试验检测了碧萝芷对血管损伤标志物内皮素-1水平的影响,内皮素-1是血管损伤的标志。34名受试者在12周内每天服用100mg碧萝芷,与43名服用安慰剂的受试者相比,内皮素-1水平降低40。一项对1289人进行的多项研究的全面综述发现,碧萝芷对治疗糖尿病视网膜病变可能有用。这篇文章的结论是,60至150mg的碧萝芷剂量有助于减缓糖尿病视网膜病变的进展,提高2型糖尿病患者的视力,提高毛细血管的强度,并减少毛细血管渗漏到视网膜中41。另一项研究考察了在二个月内每天给2型糖尿病患者服用150mg碧萝芷的效果,发现24名接受碧萝芷治疗的受试者与接受安慰剂治疗的22名受试者相比,视力提高,视网膜肿胀和增厚减少42。除了含有可以中和糖尿病引起的视网膜损伤的化合物外,碧萝芷中的一些化合物可能有助于修复受损的毛细血管39。
9.越橘:
越橘是一种与蓝莓有亲缘关系的水果。它含有多种花青素的有益化合物,被证明有助于眼睛健康43-45。从历史上看,英国飞行员在二战中吃越橘酱是为了改善他们的夜视能力,但越橘也可能对治疗视网膜病变有用46。越橘和越橘提取物可以减轻视网膜中的新生血管形成,新生血管可导致视网膜病变复杂化46-48。
10.姜黄素:
姜黄素是阿育吠陀医学重要的草药姜黄中发现的化合物。它可能预防糖尿病的一些并发症,包括视网膜病变49。姜黄素似乎能够调节参与炎症的多种蛋白质的激活,包括肿瘤坏死因子α(TNF-α)和COX-2,它们在糖尿病视网膜病变和其他眼部疾病的进展中发挥作用50。
在糖尿病视网膜病变的动物模型中,姜黄素能够保护视网膜毛细血管中的细胞免受损伤,并降低VEGF水平,有助于预防新生血管形成49,51。姜黄素还降低了糖尿病视网膜病变动物模型中的视网膜炎症标志物52。此外,它可以防止高血糖诱导的眼睛异常血管的增殖53。一项临床试验检测了每天200mg姜黄素对糖尿病视网膜病变患者的影响。接受姜黄素补充剂的受试者视网膜肿胀减少,视力提高,视网膜血流改善54。
11.银杏叶:
银杏叶提取物含有60多种生物活性化合物,可能有助于促进人类健康55。它似乎可以防止有毒化学物质对视网膜细胞的损伤,这些化学物质会损伤神经元55,56。此外,银杏叶提取物通过抑制血栓、改善血管健康、使红细胞更柔韧、使其更自由地循环,有助于改善循环55。因此,银杏叶可能能够预防糖尿病视网膜病变和早产儿视网膜病变。
在糖尿病动物模型中,银杏与白柳树皮结合可以减少炎症和视网膜细胞损伤32。在一项临床试验中,服用240mg银杏叶提取物三个月后,每天可改善2型糖尿病患者的视网膜血流量57。银杏叶在预防早产视网膜病变引起的氧气输送不足(缺氧)损伤方面也显示出了前景。在细胞培养和视网膜病变大鼠模型中,银杏叶提取物可以防止缺氧损伤和异常血管的形成55,58。
不过,银杏叶应该小心使用,因为它的血液稀释能力会导致出血风险增加,包括视网膜出血59。
12.绿茶:
绿茶能有效对抗氧化应激,而氧化应激在糖尿病视网膜病变中起着重要作用。在糖尿病视网膜病变的动物模型中,给予绿茶16周使氧化应激和炎症的几种标志物正常化。绿茶处理还保留了视网膜细胞的结构完整性60。绿茶还可以帮助糖尿病患者改善血糖控制,并可以预防老年痴呆症61,62。绿茶中的一些化合物,特别是表没食子儿茶素没食子酸盐(EGCG),可能抑制导致视网膜病变的血管异常形成63,64。
了解更多可点击其个性化综合干预方案如下:
以及参阅有关专文的更多内容:
医疗干预
主要是治疗病因,控制好血糖和高血压,有助于降低视网膜损害、防止视网膜病变进展。
治疗主要目标,视网膜病变引起的异常血管损害,包括:冷冻疗法和光凝。
参考文献:
1. Balakumar P et al. The multifaceted therapeutic potential of benfotiamine. Pharmalogical Research, 2010; 61: 482-488
2. Hammes H-P et al. Benfotiamine blocks three major pathways of hyperglycemic damage and prevents experimental diabetic retinopathy. Nature Medicine, 2003; 9(3): 294-299.
3. Karachalias N et al. Increased protein damage in renal glomeruli, retina, nerve, plasma and urine and its prevention by thiamine and benfotiamine therapy in a rat model of diabetes. Diabetologica, 2010; 53: 1506-1516.
4. Du X et al. Oral benfotiamine plus α-lipoic acid normalizes complication-causing pathways in type 1 diabetes. Diabetologia, 2008; 51: 1930-1932.
5. Chew EY. Fatty Acids and Retinopathy. The New England Journal of Medicine, 2011; 264(20): 1970-1971.
6. Jeffrey BG et al. The Role of Docosahexaenoic Acid in Retinal Function. Lipids, 2001; 36(9): 859-871.
7. Bazan NG et al. Docosahexaenoic Acid Signalolipidomics in Nutrition: Significance in Aging, Neuroinflammation, Macular Degeneration, Alzheimer’s, and Other Neurodegenerative Diseases. Annual Reviews in Nutrition, 2011; 31: 321-351.
8. Chen W et al. Anti-inflammatory Effect of Docosahexaenoic Acid on Cytokine-Induced Adhesion Molecule Expression in Human Retinal Vascular Endothelial Cells. Investigative Ophthalmology and Visual Science, 2005; 46(11): 4342-4347.
9. Bazan NG. Cell survival matters: docosahexaenoic acid signaling, neuroprotection and Photoreceptors. Trends in Neuroscience, 2006; 29(5): 263-271.
10. Mukherjee PK et al. Neuroprotectin D1: A docosahexaenoic acid-derived docosatriene protects human retinal pigment epithelial cells from oxidative stress. PNAS, 2004; 101(22): 8491-8496.
11. Sapieha P et al. 5-Lipoxygenase Metabolite 4-HDHA Is a Mediator of the Antiangiogenic Effect of w-3 Polyunsaturated Fatty Acids. Sci Transl Med. 2011 Feb 9; 3(69): 69ra12.
12. Tikhonenko M et al. N-3 Polyunsaturated Fatty Acids Prevent Diabetic Retinopathy by Inhibition of Retinal Vascular Damage and Enhanced Endothelial Progenitor Cell Reparative Function. PLOS One, 2013; 8(1)
13. Sapieha P et al. Omega-3 polyunsaturated fatty acids preserve retinal function in type 2 diabetic mice. Nutrition and Diabetes. 2012 Jul 23;2(7):e36.
14. Hard A-L et al. Nutrition, insulin-like growth factor-1 and retinopathy of prematurity. Seminars in Fetal and Neonatal Medicine, 2013; 18: 136-142.
15. Mantagos IS et al. Emerging Treatments for Retinopathy of Prematurity. Seminars in Ophthalmology, 2009; 24: 82-86.
16. Chen J et al. Current update on retinopathy of prematurity: screening and Treatment. Current Opinions in Pediatrics, 2011; 23(2): 173-178.
17. Pawlik D et al. Fish-Oil Fat Emulsion Supplementation Reduces the Risk of Retinopathy in Very Low Birth Weight Infants: A Prospective, Randomized Study. Journal of Parenteral and Enteral Nutrition. 20 Aug 2013, 38(6):711-716
18. Brazionis L et al. Plasma carotenoids and diabetic retinopathy. British Journal of Nutrition, 2009; 101: 270-277.
19. Hu B-J et al. Application of Lutein and Zeaxanthin Nonproliferative Diabetic Retinopathy. Internatinal Journal of Ophthalmology, 2011; 4(3): 303-306.
20. Li Z-Z et al. Serum lycopene levels in patients with diabetic retinopathy. European Journal of Ophthalmology, 2010; 20(4): 719-723.
21. Mactier H et al. Vitamin A Supplementation Improves Retinal Function in Infants at Risk of Retinopathy of Prematurity. The Journal of Pediatrics, 2012; 160: 954-959.
22. Moustafa SA. Zinc might protect oxidative changes in the retina and pancreas at the early stage of diabetic rats. Toxicology and Applied Pharmacology, 2004; 201: 149-155.
23. Praveena S et al. Stufy of Microelements in Diabetic Retinopathy. Journal of Evolution of Medical and Dental Sciences, 2013; 2(6): 531-537.
24. Miao X et al. Zinc and diabetic retinopathy. Journal of diabetes research. 2013;2013:425854.
25. Nebbioso M et al. Lipoic acid in animal models and clinical use in diabetic retinopathy. Expert opinion on pharmacotherapy. Sep 2013;14(13):1829-1838.
26. Lin J et al. Effect of R-(+)-a-Lipoic Acid on Experimental Diabetic Retinopathy. Diabetologia, 2006; 1089-1096.
27. Kowluru RA et al. Effect of long-term administration of alpha-lipoic acid on retinal capillary cell death and development of retinopathy in diabetic rats. Diabetes. 2004;53(12):3233-8.
28. Roberts R et al. -Lipoic Acid Corrects Late-Phase Supernormal Retinal Oxygenation Response in Experimental Diabetic Retinopathy. Invest Ophthalmol Vis Sci. 2006;47: 4077–4082).
29. Hipkiss AR. Carnosine and its possible roles in nutrition and health. Advances in food and nutrition research. 2009;57:87-154.
30. Pfister F et al. Oral Carnosine Supplementation Prevents Vascular Damage in Experimental Diabetic Retinopathy. Cellular Physiology and Biochemistry, 2011; 28: 125-136.
31. Fagiani E et al. Angiopoietins in angiogenesis. Cancer letters. Jan 1 2013;328(1):18-26.
32. Bucolo C et al. Fortified Extract of Red Berry, Ginkgo biloba, and White Willow Bark in Experimental Early Diabetic Retinopathy. J Diabetes Res. 2013:2013:432695.
33. Rahman MR et al. Diabetic Retinopathy and Homocysteine in Newly Diagnosed Type 2 Diabetes Mellitus. Delta Med Col J.Jul 2013;1(2):37-41
34. Satyanarayana A et al. Status of B-Vitamins and Homocysteine in Diabetic Retinopathy: Association with Vitamin-B12 Deficiency and Hyperhomocysteinemia. PLOS One, 2011;6(11):e26747.
35. Lim CP et al. Plasma, aqueous and vitreous homocysteine levels in proliferative diabetic retinopathy. The British journal of ophthalmology. May 2012;96(5):704-707.
36. Cahill MT et al. Meta-analysis of plasma homocysteine, serum folate, serum vitamin B(12), and thermolabile MTHFR genotype as risk factors for retinal vascular occlusive disease. American journal of ophthalmology. Dec 2003;136(6):1136-1150.
37. Sato Y et al. Relationship between metformin use, vitamin B12 deficiency, hyperhomocysteinemia and vascular complications in patients with type 2 diabetes. Endocr J. 2013;60(12):1275-80.
38. Smolek MK et al. Intervention with vitamins in patients with nonproliferative diabetic retinopathy: a pilot study. Clinical Ophthalmology, 2013; 7: 1451-1458.
39. Spadea L et al. Treatment of Cascular Retinopathies with Pycnogenol. Phytotherapy Research, 2001; 15: 219-223.
40. Liu X et al. Antidiabetic effect of PycnogenolR French maritime pine bark extract in patients with diabetes type II. Life Sciences, 2004; 75: 2505-2513.
41. Schonlau F et al. Pycnogenol for Diabetic Retinopathy. International Ophthalmology, 2002; 24: 161-171.
42. Steigerwalt R et al. Pycnogenol® Improves Microcirculation, Retinal Edema, and Visual Acuity in Early Diabetic Retinopathy. Journal of Ocular Pharmacology and Therapeutics, 2009; 25(6): 537-540.
43. Kemper KJ. Bilberry. The Longwood Herbal Task Force, 1999.
44. Bornsek SM et al. Bilberry and blueberry anthocyanins act as powerful intracellular antioxidants in mammalian cells. Food chemistry. Oct 15 2012;134(4):1878-1884.
45. Miyake S et al. Vision preservation during retinal inflammation by anthocyanin-rich bilberry extract: cellular and molecular mechanism. Lab Invest. Jan 2012;92(1):102-109.
46. Tracy TS and Kingston RL. Herbal Products: Toxicology and Clinical Pharmacology. Totowa, NJ: Humana, 2007. Print.
47. Zafra-Stone S et al. Berry Anthocyanins as Novel Antioxidants in Human Health and Disease Prevention. Moleculat Nutrition and Food Research, 2007; 51: 675-683
48. Matsunaga N et al. Vaccinium myrtillus (Bilberry) Extracts Reduce Angiogenesis In Vitro and In Vivo. eCAM, 2010; 7(1): 47-56.
49. Gupta SK et al. Curcumin Prevents Experimental Diabetic Retinopathy in Rats Through Its Hypoglycemic, Antioxidant, and Anti-Inflammatory Mechanisms. Journal of Ocular Pharmacology and Therapeutics, 2011; 27(2): 123-130.
50. Srinivasan P et al. Mining MEDLINE: Postulating a Beneficial Role for Curcumin Longa in Retinal Diseases. Biolink 2004: 33-40
51. Mrudula T et al. Effect of curcumin on hyperglycemia-induced vascular endothelial growth factor expression in streptozotocin-induced diabetic rat retina. Biochemical and Biophysical Research Comminications, 2007; 361: 528-532.
52. Kowluru RA et al. Effects of curcumin on retinal oxidative stress and inflammation in diabetes. Nutrition and Metabolism, 2007; 4: 8-15.
53. Rema M et al. Diabetic Retinopathy: An Indian Perspective. Indian Journal of Medical Research, 2007; 125: 297-310
54. Steigerwalt R et al. Meriva, a Lecithinized Curcumin Delivery System, in Diabetic Microangiopathy and Retinopathy. Panminerva Medicine, 2012; 54: 11-16
55. Oh J-H et al. Effects of Ginkgo biloba Extract on Cultured Human Retinal Pigment Epithelial Cells under Chemical Hypoxia. Current Eye Research, 2013; 38(10): 1072–1082.
56. Zaghlool SS et al. Histological and immunohistochemical study on the protective effect of Ginkgo biloba extract against glutamate-induced neurotoxicity in male albino rat retinal cells. The Egyptian Journal of Histology, 2012; 35: 176-188.
57. Huang S-Y et al. Improved haemorrheological properties by Ginkgo biloba extract (Egb 761) in type 2 diabetes mellitus complicated with retinopathy. Clinical Nutrition (2004) 23, 615–621.
58. Juarez CP et al. Experimental retinopathy of prematurity: angiostatic inhibition by nimodipine, ginkgo-biloba, and dipyridamole, and response to different growth factors. European Journal of Ophthalmology, 2000; 10(1): 51-59.
59. Fraunfelder FW. Ocular Side Effects From Herbal Medicines and Nutritional Supplements. American Journal of Ophthalmology, 2004; 138: 639-647.
60. Kumar B et al. Green tea prevents hyperglycemia-induced retinal oxidative stress and inflammation in streptozotocin-induced diabetic rats. Ophthalmic research. 2012;47(2):103-108.
61. Tsuneki H et al. Effect of green tea on blood glucose levels and serum proteomic patterns in diabetic (db/db) mice and on glucose metabolism in healthy humans. BMC Pharmacology, 2004; 4:18
62. Ho S-C et al. Comparison of anti-glycation capacities of several herbal infusions with that of green tea. Food Chemistry, 2010; 122: 768-774
63. Skopinski P et al. Suppression of angiogenic activity of sera from diabetic patients with non-proliferative retinopathy by compounds of herbal origin and sulindac sulfone. Int J Mol Med. 2004; 14(4):707-11.
64. Rodriguez SK et al. Green tea catechin, epigallocatechin-3-gallate, inhibits vascular endothelial growth factor angiogenic signaling by disrupting the formation of a receptor complex. International Journal of Cancer, 2006; 118: 1635-1644.
美国梅奥诊所
www.mayoclinic.org
美国验光协会
https://www.aoa.org
其他参考文献:详见具体的综合干预方案
免责声明和安全信息
英文名称:Retinopathy,Retinal damage,Retinal Disease
定义
视网膜病变即视网膜损伤,如不治疗和控制可严重和永久性损害视力,甚至导致失明。视觉能力依赖于视网膜健康功能,它是位于眼球后面的一层由光敏细胞和神经细胞组成的感光组织,借助于神经脉冲反射到大脑。糖尿病引起的视网膜病变是最常见的。
病因
视网膜损伤反应微血管疾病,大多由糖尿病和高血压所导致:- 糖尿病视网膜病变:高血糖引起糖毒性、细胞应激和损伤,导致微血管破坏和视网膜功能障碍,甚至促使新血管形成。与此同时,糖尿病患者眼睛微血管可能容易阻塞,这将进一步损伤并可能增加黄斑水肿,引起细胞缺氧,并诱导新的血管形成。但是,这些新血管很脆弱,易破裂泄漏,导致出血和视网膜黄斑水肿恶化等。
- 了解更多:糖尿病视网膜病变 >>
- 高血压性视网膜病变:早期是视网膜小动脉收缩、损坏,引起结缔组织分解,导致视网膜破坏,使血液和血脂蔓延到视网膜周围,引起视网膜肿胀等。
风险因素
可增加视网膜病变的风险因素包括:- 1型糖尿病,比2型糖尿病更易患上视网膜病变
- 2型糖尿病
- 长期使用胰岛素
- 高血压,随着年龄增长发病率越高
- 慢性肾脏病
症状
一般情况下,视网膜病变早期阶段是没有症状的。然而,许多糖尿病视网膜病变的早期迹象,可由医生检查出来。
当出现症状时,可能会出现宽谱视力问题,从轻度模糊到突然剧烈的视力损失,特别是在视网膜脱离或出血的情况下。
疗法
控制好血糖和高血压是治疗基础。综合疗法可包括如下:
调整饮食与生活方式
- 限制高糖、精制淀粉和高脂肪饮食。
- 饮食富含蔬菜、水果,豆类和低脂乳制品。
- 控制食盐摄入量,防止高血压。
- 戒烟或不抽烟。
- 适度饮酒,或不饮酒。
- 坚持运动锻炼,保持健康体重。
营养与草本综合干预
以下是基于循证医学和循证营养学有关文献综合的结果。
有助于防控视网膜病变营养和草本补充剂,主要包括如下:
1.苯磷硫胺:
苯磷硫胺是硫胺素(维生素B1)的衍生物。它已被证明可以减少AGEs(糖基化终产物)引发的视网膜和全身损伤1。
在糖尿病的动物模型中,苯磷硫胺给药通过改善炎症和减轻因高血糖导致的组织损伤的各种途径来预防糖尿病视网膜病变2。在另一种糖尿病动物模型中,苯磷硫胺和硫胺素能够减少视网膜和其他组织中AGEs的积聚3。在1型糖尿病患者中,每天二次补充300mg苯磷硫胺和600mg α-硫辛酸,持续28天,也被证明可以减少的AGEs积累4。
2.欧米伽-3脂肪酸:
包括欧米伽-3脂肪酸在内的多不饱和脂肪酸在身体中发挥着许多作用。有一些证据表明,ω-3脂肪酸可能在维持视网膜健康方面发挥关键作用5。DHA(一种主要的ω-3脂肪酸)在视网膜中含量很高,视网膜中DHA水平的降低与视网膜功能的改变有关。即使在DHA摄入量较低的时期,视网膜中的DHA水平也会保持不变,这进一步强调了其在视网膜组织中的重要性6。
DHA具有抗炎特性,可能能够抵消糖尿病视网膜病变中出现的一些炎症变化7,8。此外,DHA是一种名为神经保护素D1的化合物的前体,该化合物保护眼睛免受炎症损伤,并促进视网膜内细胞的存活9,10。神经保护素D1还抑制新血管的生长7。DHA本身也可以对抗视网膜中异常血管的生长11。在糖尿病动物模型中,补充ω-3有助于预防糖尿病视网膜病变12,13。
ω-3脂肪酸也可能在早产儿视网膜病变中发挥作用。在妊娠晚期,大量长链多不饱和脂肪酸通过胎盘转移到胎儿体内。早产时,婴儿的储备可能不足,这可能会影响视网膜发育14。在早产儿视网膜病变的动物模型中,在饮食中补充ω-3脂肪酸可以防止异常血管发育和视网膜病变5,14-16。一项临床试验发现,接受静脉注射富含ω-3脂肪酸的鱼油的早产儿需要视网膜病变的激光手术较少17。
3.类胡萝卜素和维生素A:
维生素A和类胡萝卜素的相关化合物对眼睛健康和功能至关重要。维生素A及其前体β-胡萝卜素是眼睛细胞吸收光线所必需的。其他类胡萝卜素,包括叶黄素、玉米黄质和番茄红素,也存在于眼睛中,对正常视力和保护眼睛免受潜在的破坏性光线和氧化应激至关重要18,19。多项研究发现,与没有视网膜病变的糖尿病患者相比,糖尿病视网膜病变患者的番茄红素、叶黄素和其他类胡萝卜素水平较低18-20。
研究已经调查了维生素A和其他类胡萝卜素作为潜在的视网膜病变治疗方法。一项临床试验发现,患有非增殖性视网膜病变的糖尿病患者在连续三个月每天补充6mg叶黄素和0.5mg玉米黄质后,视力有所改善19。一项临床试验发现,至少两周内肌肉注射10,000IU维生素A有助于改善早产儿的视网膜敏感性,进一步支持维生素A对视网膜损伤的潜在保护作用21。
4.锌:
锌在眼部含量浓度较高,可以帮助减少眼睛的氧化损伤22。糖尿病视网膜病变患者的锌水平通常低于健康人23,24。补充锌可能有助于预防糖尿病视网膜病变并延缓其进展。锌还有助于改善血糖控制,抑制异常视网膜血管的生长,防止血管受损和渗漏24。在糖尿病大鼠模型中,补锌抑制了VEGF的水平,VEGF是一种参与新生血管形成的化学物质24。
5.硫辛酸:
硫辛酸是一种“万能”的抗氧化剂,已知可提高2型糖尿病患者的胰岛素敏感性,并能预防糖尿病视网膜病变25。它可以帮助恢复视网膜细胞内的抗氧化防御26。对糖尿病动物模型的研究发现,给予α-硫辛酸可以减少被自由基损伤的分子的积累,并有助于保护视网膜中的血管27,28。硫辛酸似乎还能抑制参与新血管形成的生长因子的产生,这是糖尿病视网膜病变进展的主要特征25。
6.肌肽:
肌肽是一种主要由骨骼肌产生的化合物,由两种氨基酸(丙氨酸和组氨酸)组成。它能够阻断AGEs的产生,减轻氧化应激和糖尿病的其他并发症29。
在糖尿病视网膜病变的动物模型中,肌肽补充剂除了抑制AGEs外,还通过其他机制延缓白内障的形成,保护视网膜毛细血管免受高血糖损伤。例如,研究人员发现肌肽的保护作用与预防高血糖诱导的一种名为Ang-2的生长因子增加有关(Ang-2与VEGF结合会导致血管损伤和新生血管形成)30,31。在另一种糖尿病视网膜病变模型中,肌肽与白柳树皮提取物、α-硫辛酸和银杏叶联合保护视网膜细胞免受损伤32。
7.维生素B族:
维生素B12可能通过帮助保持低同型半胱氨酸水平来预防视网膜病变。同型半胱氨酸是一种会损伤血管的氨基酸。糖尿病患者对高同型半胱氨酸水平(高血同)引起的血管损伤特别敏感,因为糖尿病会导致同型半胱氨酸的化学变化,使该分子毒性更强33。中和同型半胱氨酸的酶需要维生素B12才能发挥作用;因此,维生素B12缺乏会导致同型半胱氨酸水平升高,并导致糖尿病视网膜病变34。
患有糖尿病视网膜病变的人通常具有较高的同型半胱氨酸水平和较低的维生素B12水平,这表明维生素B12缺乏与糖尿病视网膜病变之间存在联系33,34。一项研究发现,增殖性糖尿病神经病变患者的同型半胱氨酸水平估计比对照组高出约30%35。在对300名2型糖尿病受试者进行的一项类似研究中,维生素B12和叶酸水平较低与同型半胱氨酸水平升高有关,而在患有糖尿病视网膜病变的研究人群中,同型半胱氨酸的水平尤其高34。另一项研究发现,614名患有视网膜血管疾病的受试者的血浆总同型半胱氨酸水平高于762名对照受试者36。
重要的是,一些糖尿病治疗药物,如二甲双胍可能引起维生素B12下降,增加同型半胱氨酸水平。这种与治疗相关的维生素B12缺乏可能会增加糖尿病视网膜病变的风险,这突出了糖尿病患者补充维生素B12的重要性37。其他B族维生素也可能在预防糖尿病视网膜病变方面发挥协同作用。一项研究发现,维生素B12、叶酸和5’-磷酸吡哆醛(活性维生素B6)的组合在减少非增殖性糖尿病视网膜病变患者的视网膜水肿和提高光敏感性方面具有有益效果38。
8.碧萝芷:
碧萝芷是从法国海松树皮中分离的提取物,已被研究用于治疗糖尿病视网膜病变39。碧萝芷的一个好处是它可以帮助降低血糖水平。此外,碧萝芷可以保护视网膜中的毛细血管免受损伤。
一项研究77名2型糖尿病患者的临床试验检测了碧萝芷对血管损伤标志物内皮素-1水平的影响,内皮素-1是血管损伤的标志。34名受试者在12周内每天服用100mg碧萝芷,与43名服用安慰剂的受试者相比,内皮素-1水平降低40。一项对1289人进行的多项研究的全面综述发现,碧萝芷对治疗糖尿病视网膜病变可能有用。这篇文章的结论是,60至150mg的碧萝芷剂量有助于减缓糖尿病视网膜病变的进展,提高2型糖尿病患者的视力,提高毛细血管的强度,并减少毛细血管渗漏到视网膜中41。另一项研究考察了在二个月内每天给2型糖尿病患者服用150mg碧萝芷的效果,发现24名接受碧萝芷治疗的受试者与接受安慰剂治疗的22名受试者相比,视力提高,视网膜肿胀和增厚减少42。除了含有可以中和糖尿病引起的视网膜损伤的化合物外,碧萝芷中的一些化合物可能有助于修复受损的毛细血管39。
9.越橘:
越橘是一种与蓝莓有亲缘关系的水果。它含有多种花青素的有益化合物,被证明有助于眼睛健康43-45。从历史上看,英国飞行员在二战中吃越橘酱是为了改善他们的夜视能力,但越橘也可能对治疗视网膜病变有用46。越橘和越橘提取物可以减轻视网膜中的新生血管形成,新生血管可导致视网膜病变复杂化46-48。
10.姜黄素:
姜黄素是阿育吠陀医学重要的草药姜黄中发现的化合物。它可能预防糖尿病的一些并发症,包括视网膜病变49。姜黄素似乎能够调节参与炎症的多种蛋白质的激活,包括肿瘤坏死因子α(TNF-α)和COX-2,它们在糖尿病视网膜病变和其他眼部疾病的进展中发挥作用50。
在糖尿病视网膜病变的动物模型中,姜黄素能够保护视网膜毛细血管中的细胞免受损伤,并降低VEGF水平,有助于预防新生血管形成49,51。姜黄素还降低了糖尿病视网膜病变动物模型中的视网膜炎症标志物52。此外,它可以防止高血糖诱导的眼睛异常血管的增殖53。一项临床试验检测了每天200mg姜黄素对糖尿病视网膜病变患者的影响。接受姜黄素补充剂的受试者视网膜肿胀减少,视力提高,视网膜血流改善54。
11.银杏叶:
银杏叶提取物含有60多种生物活性化合物,可能有助于促进人类健康55。它似乎可以防止有毒化学物质对视网膜细胞的损伤,这些化学物质会损伤神经元55,56。此外,银杏叶提取物通过抑制血栓、改善血管健康、使红细胞更柔韧、使其更自由地循环,有助于改善循环55。因此,银杏叶可能能够预防糖尿病视网膜病变和早产儿视网膜病变。
在糖尿病动物模型中,银杏与白柳树皮结合可以减少炎症和视网膜细胞损伤32。在一项临床试验中,服用240mg银杏叶提取物三个月后,每天可改善2型糖尿病患者的视网膜血流量57。银杏叶在预防早产视网膜病变引起的氧气输送不足(缺氧)损伤方面也显示出了前景。在细胞培养和视网膜病变大鼠模型中,银杏叶提取物可以防止缺氧损伤和异常血管的形成55,58。
不过,银杏叶应该小心使用,因为它的血液稀释能力会导致出血风险增加,包括视网膜出血59。
12.绿茶:
绿茶能有效对抗氧化应激,而氧化应激在糖尿病视网膜病变中起着重要作用。在糖尿病视网膜病变的动物模型中,给予绿茶16周使氧化应激和炎症的几种标志物正常化。绿茶处理还保留了视网膜细胞的结构完整性60。绿茶还可以帮助糖尿病患者改善血糖控制,并可以预防老年痴呆症61,62。绿茶中的一些化合物,特别是表没食子儿茶素没食子酸盐(EGCG),可能抑制导致视网膜病变的血管异常形成63,64。
了解更多可点击其个性化综合干预方案如下:
- 视网膜病管理:
- 糖尿病视网膜病管理:
- 高血压视网膜病管理:
以及参阅有关专文的更多内容:
医疗干预
主要是治疗病因,控制好血糖和高血压,有助于降低视网膜损害、防止视网膜病变进展。
治疗主要目标,视网膜病变引起的异常血管损害,包括:冷冻疗法和光凝。
预防
管理和控制好相关的慢性病如糖尿病、高血压等是关键。参考文献:
1. Balakumar P et al. The multifaceted therapeutic potential of benfotiamine. Pharmalogical Research, 2010; 61: 482-488
2. Hammes H-P et al. Benfotiamine blocks three major pathways of hyperglycemic damage and prevents experimental diabetic retinopathy. Nature Medicine, 2003; 9(3): 294-299.
3. Karachalias N et al. Increased protein damage in renal glomeruli, retina, nerve, plasma and urine and its prevention by thiamine and benfotiamine therapy in a rat model of diabetes. Diabetologica, 2010; 53: 1506-1516.
4. Du X et al. Oral benfotiamine plus α-lipoic acid normalizes complication-causing pathways in type 1 diabetes. Diabetologia, 2008; 51: 1930-1932.
5. Chew EY. Fatty Acids and Retinopathy. The New England Journal of Medicine, 2011; 264(20): 1970-1971.
6. Jeffrey BG et al. The Role of Docosahexaenoic Acid in Retinal Function. Lipids, 2001; 36(9): 859-871.
7. Bazan NG et al. Docosahexaenoic Acid Signalolipidomics in Nutrition: Significance in Aging, Neuroinflammation, Macular Degeneration, Alzheimer’s, and Other Neurodegenerative Diseases. Annual Reviews in Nutrition, 2011; 31: 321-351.
8. Chen W et al. Anti-inflammatory Effect of Docosahexaenoic Acid on Cytokine-Induced Adhesion Molecule Expression in Human Retinal Vascular Endothelial Cells. Investigative Ophthalmology and Visual Science, 2005; 46(11): 4342-4347.
9. Bazan NG. Cell survival matters: docosahexaenoic acid signaling, neuroprotection and Photoreceptors. Trends in Neuroscience, 2006; 29(5): 263-271.
10. Mukherjee PK et al. Neuroprotectin D1: A docosahexaenoic acid-derived docosatriene protects human retinal pigment epithelial cells from oxidative stress. PNAS, 2004; 101(22): 8491-8496.
11. Sapieha P et al. 5-Lipoxygenase Metabolite 4-HDHA Is a Mediator of the Antiangiogenic Effect of w-3 Polyunsaturated Fatty Acids. Sci Transl Med. 2011 Feb 9; 3(69): 69ra12.
12. Tikhonenko M et al. N-3 Polyunsaturated Fatty Acids Prevent Diabetic Retinopathy by Inhibition of Retinal Vascular Damage and Enhanced Endothelial Progenitor Cell Reparative Function. PLOS One, 2013; 8(1)
13. Sapieha P et al. Omega-3 polyunsaturated fatty acids preserve retinal function in type 2 diabetic mice. Nutrition and Diabetes. 2012 Jul 23;2(7):e36.
14. Hard A-L et al. Nutrition, insulin-like growth factor-1 and retinopathy of prematurity. Seminars in Fetal and Neonatal Medicine, 2013; 18: 136-142.
15. Mantagos IS et al. Emerging Treatments for Retinopathy of Prematurity. Seminars in Ophthalmology, 2009; 24: 82-86.
16. Chen J et al. Current update on retinopathy of prematurity: screening and Treatment. Current Opinions in Pediatrics, 2011; 23(2): 173-178.
17. Pawlik D et al. Fish-Oil Fat Emulsion Supplementation Reduces the Risk of Retinopathy in Very Low Birth Weight Infants: A Prospective, Randomized Study. Journal of Parenteral and Enteral Nutrition. 20 Aug 2013, 38(6):711-716
18. Brazionis L et al. Plasma carotenoids and diabetic retinopathy. British Journal of Nutrition, 2009; 101: 270-277.
19. Hu B-J et al. Application of Lutein and Zeaxanthin Nonproliferative Diabetic Retinopathy. Internatinal Journal of Ophthalmology, 2011; 4(3): 303-306.
20. Li Z-Z et al. Serum lycopene levels in patients with diabetic retinopathy. European Journal of Ophthalmology, 2010; 20(4): 719-723.
21. Mactier H et al. Vitamin A Supplementation Improves Retinal Function in Infants at Risk of Retinopathy of Prematurity. The Journal of Pediatrics, 2012; 160: 954-959.
22. Moustafa SA. Zinc might protect oxidative changes in the retina and pancreas at the early stage of diabetic rats. Toxicology and Applied Pharmacology, 2004; 201: 149-155.
23. Praveena S et al. Stufy of Microelements in Diabetic Retinopathy. Journal of Evolution of Medical and Dental Sciences, 2013; 2(6): 531-537.
24. Miao X et al. Zinc and diabetic retinopathy. Journal of diabetes research. 2013;2013:425854.
25. Nebbioso M et al. Lipoic acid in animal models and clinical use in diabetic retinopathy. Expert opinion on pharmacotherapy. Sep 2013;14(13):1829-1838.
26. Lin J et al. Effect of R-(+)-a-Lipoic Acid on Experimental Diabetic Retinopathy. Diabetologia, 2006; 1089-1096.
27. Kowluru RA et al. Effect of long-term administration of alpha-lipoic acid on retinal capillary cell death and development of retinopathy in diabetic rats. Diabetes. 2004;53(12):3233-8.
28. Roberts R et al. -Lipoic Acid Corrects Late-Phase Supernormal Retinal Oxygenation Response in Experimental Diabetic Retinopathy. Invest Ophthalmol Vis Sci. 2006;47: 4077–4082).
29. Hipkiss AR. Carnosine and its possible roles in nutrition and health. Advances in food and nutrition research. 2009;57:87-154.
30. Pfister F et al. Oral Carnosine Supplementation Prevents Vascular Damage in Experimental Diabetic Retinopathy. Cellular Physiology and Biochemistry, 2011; 28: 125-136.
31. Fagiani E et al. Angiopoietins in angiogenesis. Cancer letters. Jan 1 2013;328(1):18-26.
32. Bucolo C et al. Fortified Extract of Red Berry, Ginkgo biloba, and White Willow Bark in Experimental Early Diabetic Retinopathy. J Diabetes Res. 2013:2013:432695.
33. Rahman MR et al. Diabetic Retinopathy and Homocysteine in Newly Diagnosed Type 2 Diabetes Mellitus. Delta Med Col J.Jul 2013;1(2):37-41
34. Satyanarayana A et al. Status of B-Vitamins and Homocysteine in Diabetic Retinopathy: Association with Vitamin-B12 Deficiency and Hyperhomocysteinemia. PLOS One, 2011;6(11):e26747.
35. Lim CP et al. Plasma, aqueous and vitreous homocysteine levels in proliferative diabetic retinopathy. The British journal of ophthalmology. May 2012;96(5):704-707.
36. Cahill MT et al. Meta-analysis of plasma homocysteine, serum folate, serum vitamin B(12), and thermolabile MTHFR genotype as risk factors for retinal vascular occlusive disease. American journal of ophthalmology. Dec 2003;136(6):1136-1150.
37. Sato Y et al. Relationship between metformin use, vitamin B12 deficiency, hyperhomocysteinemia and vascular complications in patients with type 2 diabetes. Endocr J. 2013;60(12):1275-80.
38. Smolek MK et al. Intervention with vitamins in patients with nonproliferative diabetic retinopathy: a pilot study. Clinical Ophthalmology, 2013; 7: 1451-1458.
39. Spadea L et al. Treatment of Cascular Retinopathies with Pycnogenol. Phytotherapy Research, 2001; 15: 219-223.
40. Liu X et al. Antidiabetic effect of PycnogenolR French maritime pine bark extract in patients with diabetes type II. Life Sciences, 2004; 75: 2505-2513.
41. Schonlau F et al. Pycnogenol for Diabetic Retinopathy. International Ophthalmology, 2002; 24: 161-171.
42. Steigerwalt R et al. Pycnogenol® Improves Microcirculation, Retinal Edema, and Visual Acuity in Early Diabetic Retinopathy. Journal of Ocular Pharmacology and Therapeutics, 2009; 25(6): 537-540.
43. Kemper KJ. Bilberry. The Longwood Herbal Task Force, 1999.
44. Bornsek SM et al. Bilberry and blueberry anthocyanins act as powerful intracellular antioxidants in mammalian cells. Food chemistry. Oct 15 2012;134(4):1878-1884.
45. Miyake S et al. Vision preservation during retinal inflammation by anthocyanin-rich bilberry extract: cellular and molecular mechanism. Lab Invest. Jan 2012;92(1):102-109.
46. Tracy TS and Kingston RL. Herbal Products: Toxicology and Clinical Pharmacology. Totowa, NJ: Humana, 2007. Print.
47. Zafra-Stone S et al. Berry Anthocyanins as Novel Antioxidants in Human Health and Disease Prevention. Moleculat Nutrition and Food Research, 2007; 51: 675-683
48. Matsunaga N et al. Vaccinium myrtillus (Bilberry) Extracts Reduce Angiogenesis In Vitro and In Vivo. eCAM, 2010; 7(1): 47-56.
49. Gupta SK et al. Curcumin Prevents Experimental Diabetic Retinopathy in Rats Through Its Hypoglycemic, Antioxidant, and Anti-Inflammatory Mechanisms. Journal of Ocular Pharmacology and Therapeutics, 2011; 27(2): 123-130.
50. Srinivasan P et al. Mining MEDLINE: Postulating a Beneficial Role for Curcumin Longa in Retinal Diseases. Biolink 2004: 33-40
51. Mrudula T et al. Effect of curcumin on hyperglycemia-induced vascular endothelial growth factor expression in streptozotocin-induced diabetic rat retina. Biochemical and Biophysical Research Comminications, 2007; 361: 528-532.
52. Kowluru RA et al. Effects of curcumin on retinal oxidative stress and inflammation in diabetes. Nutrition and Metabolism, 2007; 4: 8-15.
53. Rema M et al. Diabetic Retinopathy: An Indian Perspective. Indian Journal of Medical Research, 2007; 125: 297-310
54. Steigerwalt R et al. Meriva, a Lecithinized Curcumin Delivery System, in Diabetic Microangiopathy and Retinopathy. Panminerva Medicine, 2012; 54: 11-16
55. Oh J-H et al. Effects of Ginkgo biloba Extract on Cultured Human Retinal Pigment Epithelial Cells under Chemical Hypoxia. Current Eye Research, 2013; 38(10): 1072–1082.
56. Zaghlool SS et al. Histological and immunohistochemical study on the protective effect of Ginkgo biloba extract against glutamate-induced neurotoxicity in male albino rat retinal cells. The Egyptian Journal of Histology, 2012; 35: 176-188.
57. Huang S-Y et al. Improved haemorrheological properties by Ginkgo biloba extract (Egb 761) in type 2 diabetes mellitus complicated with retinopathy. Clinical Nutrition (2004) 23, 615–621.
58. Juarez CP et al. Experimental retinopathy of prematurity: angiostatic inhibition by nimodipine, ginkgo-biloba, and dipyridamole, and response to different growth factors. European Journal of Ophthalmology, 2000; 10(1): 51-59.
59. Fraunfelder FW. Ocular Side Effects From Herbal Medicines and Nutritional Supplements. American Journal of Ophthalmology, 2004; 138: 639-647.
60. Kumar B et al. Green tea prevents hyperglycemia-induced retinal oxidative stress and inflammation in streptozotocin-induced diabetic rats. Ophthalmic research. 2012;47(2):103-108.
61. Tsuneki H et al. Effect of green tea on blood glucose levels and serum proteomic patterns in diabetic (db/db) mice and on glucose metabolism in healthy humans. BMC Pharmacology, 2004; 4:18
62. Ho S-C et al. Comparison of anti-glycation capacities of several herbal infusions with that of green tea. Food Chemistry, 2010; 122: 768-774
63. Skopinski P et al. Suppression of angiogenic activity of sera from diabetic patients with non-proliferative retinopathy by compounds of herbal origin and sulindac sulfone. Int J Mol Med. 2004; 14(4):707-11.
64. Rodriguez SK et al. Green tea catechin, epigallocatechin-3-gallate, inhibits vascular endothelial growth factor angiogenic signaling by disrupting the formation of a receptor complex. International Journal of Cancer, 2006; 118: 1635-1644.
参考来源:
美国梅奥诊所
www.mayoclinic.org
美国验光协会
https://www.aoa.org
其他参考文献:详见具体的综合干预方案
免责声明和安全信息
- 本信息(包括任何附带资料)不是为了取代医生或有关合格从业人士的建议或忠告。
- 任何人如果想要对本文涉及的药物、饮食、运动或其他生活方式的使用、或改变调整,以预防或治疗某一特定健康状况或疾病,应首先咨询医生或有关合格从业人士,并获得他/她们的许可。妊娠和哺乳妇女在使用本网站任何内容前,尤其应征求医生的意见。
- 除非另有说明,本网站所述内容仅适用于成人。
- 本网站所推荐的任何产品,消费者应该以实际的产品标签内容为准,尤其应关注重要的安全信息以及产品最新信息,包括剂量、使用方法和禁忌症等。
- 由于循证医学研究、文献及有关产品处于不断的变化中,本网站工作人员将尽力更新。
- 本网站不能保证所载文章内容、综合干预方案以及相关成分或产品述及的健康益处,也不承担任何责任。

